によると ロイター日本の加藤勝信厚生労働大臣は、厚生労働省の理事会が承認した経口薬Xocova(フマル酸エンシトレルビル)に関する決定を発表した。
加藤氏は「ゾコバという薬剤が、新たな治療選択肢としてSARS-CoV-2ウイルスの予防対策に貢献することを期待している」と述べた。 しかし同氏は、ショコバは妊婦には適応されないとも述べた。
承認の遅れにもかかわらず、塩野義製薬は先月、通年の売上高予想を引き上げた。 同社は、この薬の承認を待って約100万回分を政府に販売する契約を結んだ。
塩野義製薬の会長兼最高経営責任者(CEO)手代木功氏が2019年6月11日、東京でロイターのインタビューに応じた。写真:ロイター
塩野義製薬の株価は承認間近との報道を受け、2.77%高の7,171ポイントで取引を終えた。
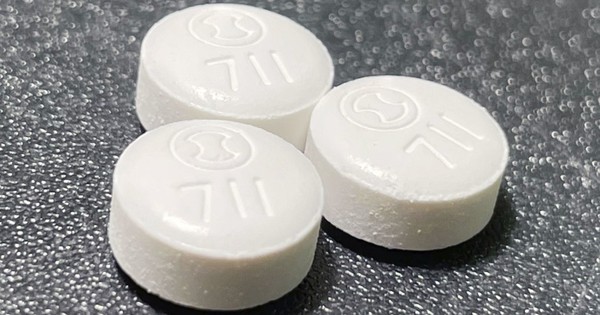
Xocovaは、12歳以上の軽度の症状を持つ新型コロナウイルス感染症患者を対象とし、5日間で7錠を投与する。 今年5月に創設された日本政府の緊急承認制度で承認された初めての医薬品となる。
ページによると 共同通信 日本では、同国の毎日の新型コロナウイルス感染者数が再び増加していることを受けて、この決定が下された。 報告書によると、11月22日の全国の感染者数は合計12万4004人で、先週から約1万8000人増加した。 死者数は計178人となった。
東京都では1万2758人の感染者を記録し、北海道、岩手県、東北地方の山形県では新たな記録を記録した。
記者会見した加藤氏は「流通体制が整い次第、12月上旬に配布を開始する予定だ」と述べた。
これに先立ち、7月には塩野義製薬の対応を受けて厚生省委員会が同薬の緊急認可を延期した。 その有効性は中期臨床試験では証明できませんでした。

塩野義製薬の新型コロナウイルス感染症用経口薬「Xocova」 写真提供:塩野義製薬
しかし、試験の最終段階でオミクロン株に特徴的な5つの症状(鼻水、喉の痛み、咳、発熱、倦怠感)を分析したところ、この薬により症状が8~7日間軽減されたことが判明した。
最終段階は日本、韓国、ベトナムで実施され、この薬は新型コロナウイルス感染症の軽度または中等度の症状を持つ患者を対象に1日1回、5日間使用される。
医薬品医療機器総合機構は、塩野義製薬が提出した後期臨床試験結果から「この薬が有効であると考えるのに十分な情報が得られた」と述べた。